Expo
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
Imagenología
Cuidados CriticosTéc. QuirúrgicaCuidados de PacientesTIPruebas POC
Eventos
Webinars

- Monitorear las esporas de hongos en el aire podría ayudar a predecir los picos de COVID-19 y gripe
- Nuevo sistema mide el sodio en sangre sin agujas
- Datos de sueño de un dispositivo portátil podrían ayudar a predecir el parto prematuro
- Herramienta de IA interpreta ecocardiogramas en minutos
- Conector de catéter electroquímico previene infecciones del torrente sanguíneo
- Nueva sonda de imagen revolucionará la cirugía del cáncer cerebral
- Nueva tecnología duplica la tasa de éxito en la eliminación de coágulos sanguíneos
- La ablación quirúrgica durante la cirugía de bypass coronario mejora la supervivencia en pacientes con fibrilación auricular
- Nueva tecnología de baterías proporciona energía adicional a los dispositivos médicos implantables.
- Nuevo modelo revela la colocación óptima de tornillos ortopédicos en fracturas
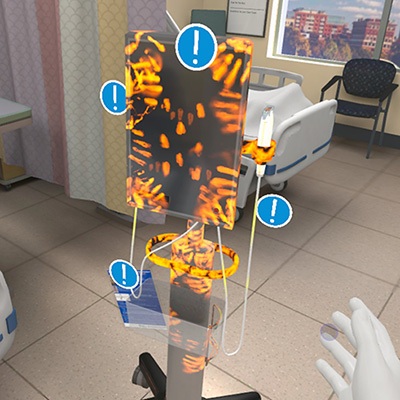
- Herramienta de capacitación en realidad virtual combate la contaminación de equipos médicos portátiles
- Plataforma de biosensores portátiles reducirá infecciones adquiridas en el hospital
- Tecnología portátil de luz germicida, única en su tipo, desinfecta superficies clínicas de alto contacto en segundos
- Solución de optimización de la capacidad quirúrgica ayuda a hospitales a impulsar utilización de quirófanos
- Innovación revolucionaria en esterilización de instrumentos quirúrgicos mejora significativamente rendimiento del quirófano
- Medtronic se asocia con Corsano para ampliar su portafolio de atención aguda y monitorización en Europa
- Colaboración ampliada transformará la tecnología en quirófanos mediante IA y automatización
- Boston Scientific adquiere la empresa de dispositivos médicos SoniVie
- Teleflex adquirirá el negocio de intervención vascular de BIOTRONIK
- El Congreso Mundial de Hospitales de 2026 se celebrará en Seúl
- Los relojes inteligentes podrían detectar la insuficiencia cardíaca congestiva
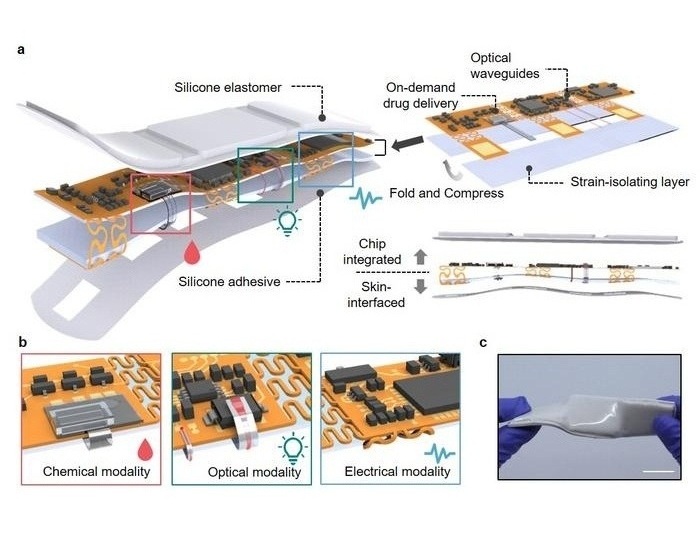
- Un parche inteligente versátil combina monitoreo de salud y administración de fármacos
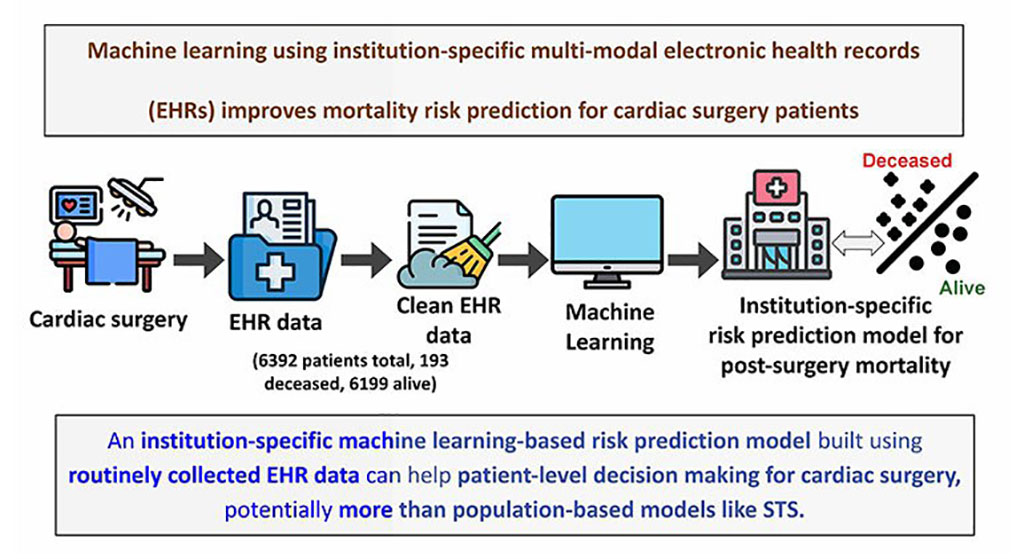
- Modelo de aprendizaje automático mejora predicción del riesgo de mortalidad para pacientes de cirugía cardíaca
- Colaboración estratégica para desarrollar e integrar IA generativa en el cuidado de la salud
- Solución de quirófanos habilitada para IA ayuda a hospitales a maximizar la utilización y desbloquear la capacidad
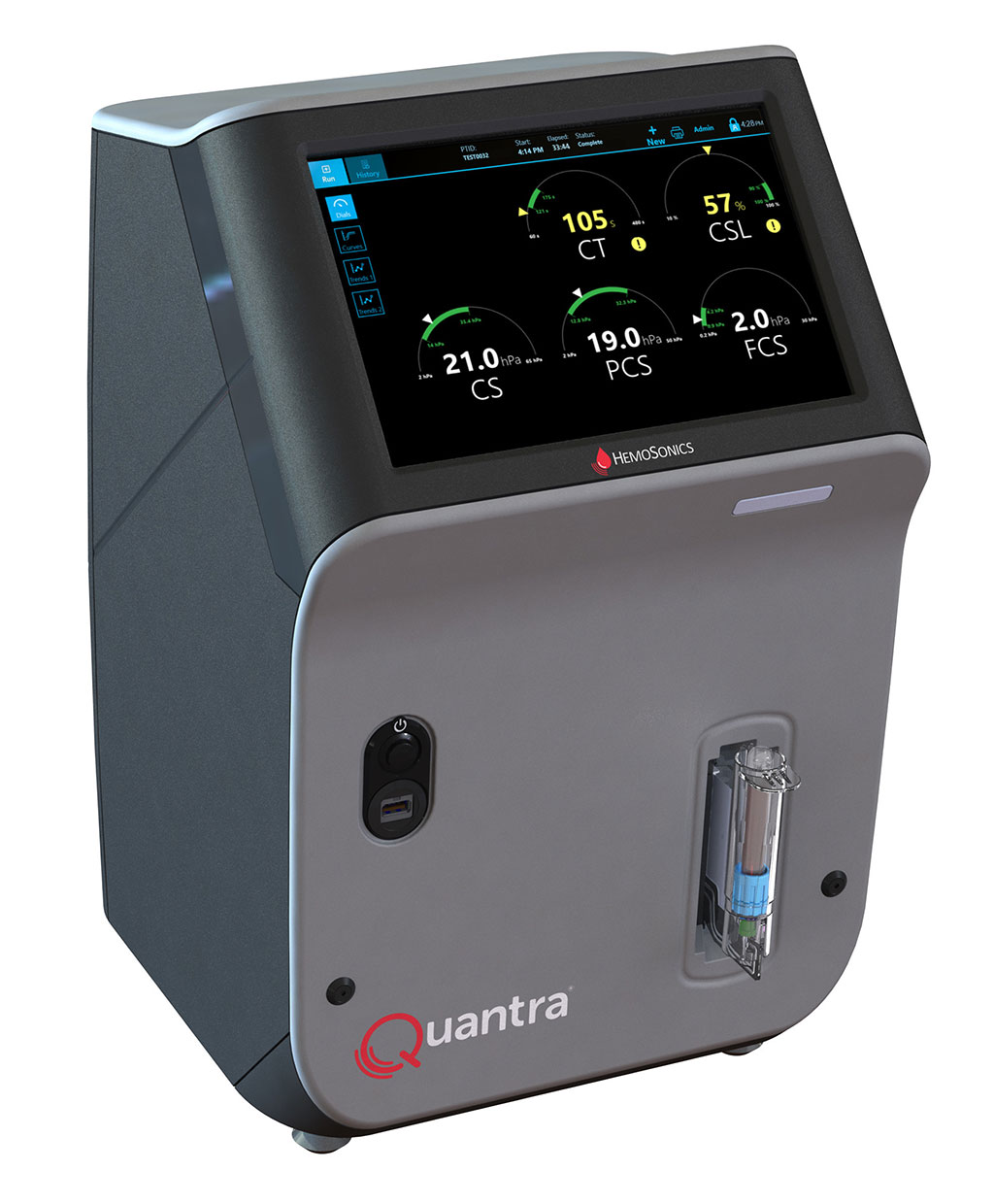
- Sistema de hemostasia de sangre total POC de última generación reconoce necesidades específicas de servicios de emergencia y quirófanos
- Laboratorio portátil permitirá identificación de infecciones bacterianas más rápida y económica en el punto de necesidad
- Mercado mundial de pruebas de cabecera será testigo de perspectivas prometedoras en cuidados intensivos
- Mercado mundial de diagnóstico de sepsis impulsado por el aumento de enfermedades adquiridas en hospitales

 Expo
Expo
- Monitorear las esporas de hongos en el aire podría ayudar a predecir los picos de COVID-19 y gripe
- Nuevo sistema mide el sodio en sangre sin agujas
- Datos de sueño de un dispositivo portátil podrían ayudar a predecir el parto prematuro
- Herramienta de IA interpreta ecocardiogramas en minutos
- Conector de catéter electroquímico previene infecciones del torrente sanguíneo
- Nueva sonda de imagen revolucionará la cirugía del cáncer cerebral
- Nueva tecnología duplica la tasa de éxito en la eliminación de coágulos sanguíneos
- La ablación quirúrgica durante la cirugía de bypass coronario mejora la supervivencia en pacientes con fibrilación auricular
- Nueva tecnología de baterías proporciona energía adicional a los dispositivos médicos implantables.
- Nuevo modelo revela la colocación óptima de tornillos ortopédicos en fracturas
- Herramienta de capacitación en realidad virtual combate la contaminación de equipos médicos portátiles
- Plataforma de biosensores portátiles reducirá infecciones adquiridas en el hospital
- Tecnología portátil de luz germicida, única en su tipo, desinfecta superficies clínicas de alto contacto en segundos
- Solución de optimización de la capacidad quirúrgica ayuda a hospitales a impulsar utilización de quirófanos
- Innovación revolucionaria en esterilización de instrumentos quirúrgicos mejora significativamente rendimiento del quirófano
- Medtronic se asocia con Corsano para ampliar su portafolio de atención aguda y monitorización en Europa
- Colaboración ampliada transformará la tecnología en quirófanos mediante IA y automatización
- Boston Scientific adquiere la empresa de dispositivos médicos SoniVie
- Teleflex adquirirá el negocio de intervención vascular de BIOTRONIK
- El Congreso Mundial de Hospitales de 2026 se celebrará en Seúl
- Los relojes inteligentes podrían detectar la insuficiencia cardíaca congestiva
- Un parche inteligente versátil combina monitoreo de salud y administración de fármacos
- Modelo de aprendizaje automático mejora predicción del riesgo de mortalidad para pacientes de cirugía cardíaca
- Colaboración estratégica para desarrollar e integrar IA generativa en el cuidado de la salud
- Solución de quirófanos habilitada para IA ayuda a hospitales a maximizar la utilización y desbloquear la capacidad
- China aprueba la primera vacuna inhalable contra la COVID-19 del mundo
- Vacuna en parche contra la COVID-19 combate variantes del SARS-CoV-2 mejor que las agujas
- Pruebas de viscosidad sanguínea predicen riesgo de muerte en pacientes hospitalizados con COVID-19
- ‘Computadora Covid’ usa IA para detectar COVID-19 en exámenes de TC de tórax
- Técnica de resonancia magnética muestra la causa de los síntomas de COVID prolongada
- Sistema de hemostasia de sangre total POC de última generación reconoce necesidades específicas de servicios de emergencia y quirófanos
- Laboratorio portátil permitirá identificación de infecciones bacterianas más rápida y económica en el punto de necesidad
- Mercado mundial de pruebas de cabecera será testigo de perspectivas prometedoras en cuidados intensivos
- Mercado mundial de diagnóstico de sepsis impulsado por el aumento de enfermedades adquiridas en hospitales