Expo
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
Imagenología
Cuidados CriticosTéc. QuirúrgicaCuidados de PacientesTIPruebas POCNegocios
Eventos
Webinars

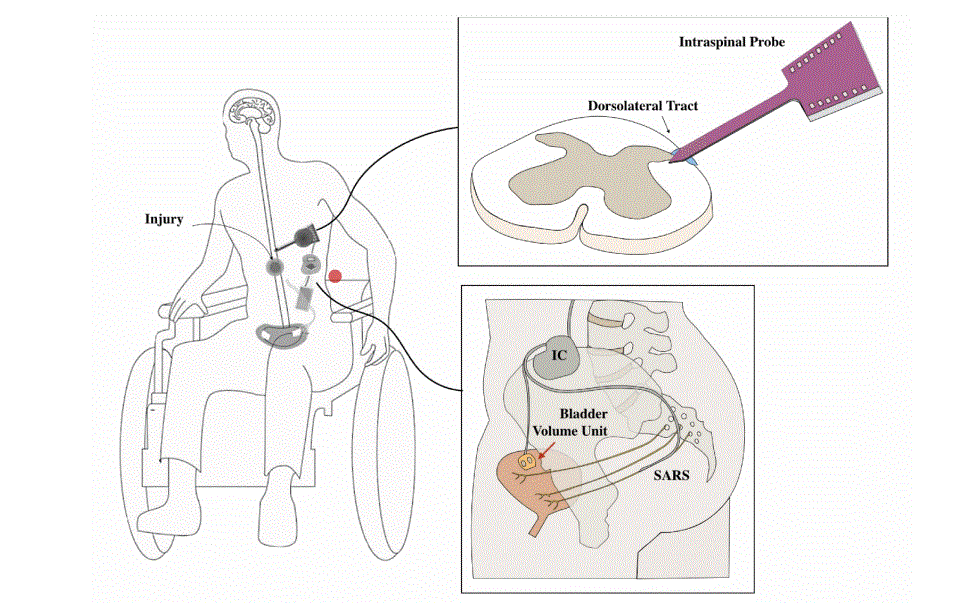
- Interfaz de médula espinal restaura el control de la vejiga en estudio preclínico
- Sistema de control magnético permite la navegación precisa de dispositivos médicos miniaturizados
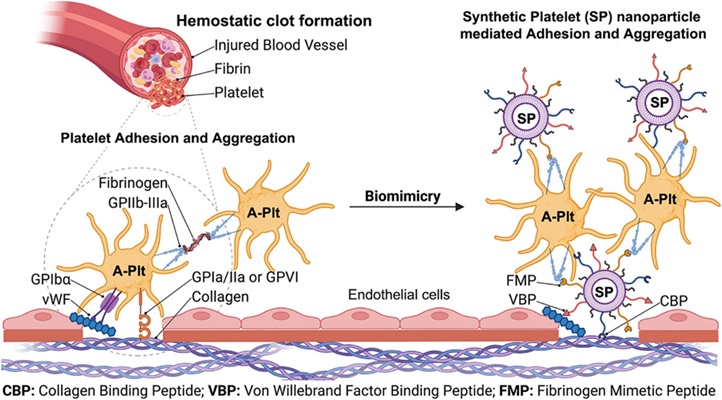
- Plaquetas sintéticas estables a temperatura ambiente podrían permitir el control prehospitalario de hemorragias
- Dispositivo de filtración sanguínea podría prolongar el embarazo en la preeclampsia temprana grave
- Sensor craneal no invasivo detecta el deterioro temprano en lesiones cerebrales agudas
- Nueva herramienta de IA predice complicaciones antes de la cirugía de cáncer de pulmón
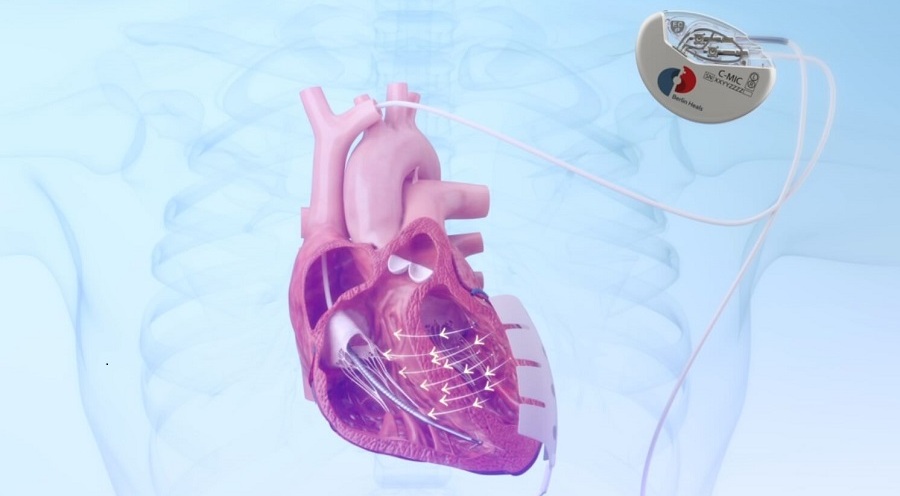
- Dispositivo cardíaco de microcorriente menos invasivo mejora los resultados en insuficiencia cardíaca
- El trasplante parcial de corazón permite el reemplazo de válvulas con capacidad de crecimiento en niños
- Cirugía temprana de “entrenamiento cardíaco” promueve la regeneración en la insuficiencia cardíaca pediátrica
- Implante inteligente para fracturas monitoriza la curación y proporciona soporte adaptativo
- Dispositivo automático de lavado de vías intravenosas mejora la atención en infusiones
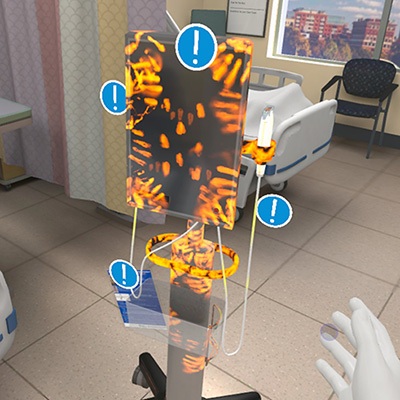
- Herramienta de capacitación en realidad virtual combate la contaminación de equipos médicos portátiles
- Plataforma de biosensores portátiles reducirá infecciones adquiridas en el hospital
- Tecnología portátil de luz germicida, única en su tipo, desinfecta superficies clínicas de alto contacto en segundos
- Solución de optimización de la capacidad quirúrgica ayuda a hospitales a impulsar utilización de quirófanos
- Sinocare presenta soluciones integradas de salud digital basadas en IA en CMEF
- GE HealthCare y Medtronic amplían su alianza con la integración de imágenes intraoperatorias.
- GE HealthCare lidera una importante iniciativa europea para impulsar la atención cardio-oncológica
- Philips y Masimo se asocian para impulsar las tecnologías de monitorización de pacientes
- B. Braun adquiere la empresa de microcirugía digital True Digital Surgery
- Herramienta basada en HCE predice el fallo del injerto tras un trasplante de riñón
- Nanopartículas imprimibles permiten la producción masiva de biosensores portátiles
- Los relojes inteligentes podrían detectar la insuficiencia cardíaca congestiva
- Un parche inteligente versátil combina monitoreo de salud y administración de fármacos
- Modelo de aprendizaje automático mejora predicción del riesgo de mortalidad para pacientes de cirugía cardíaca
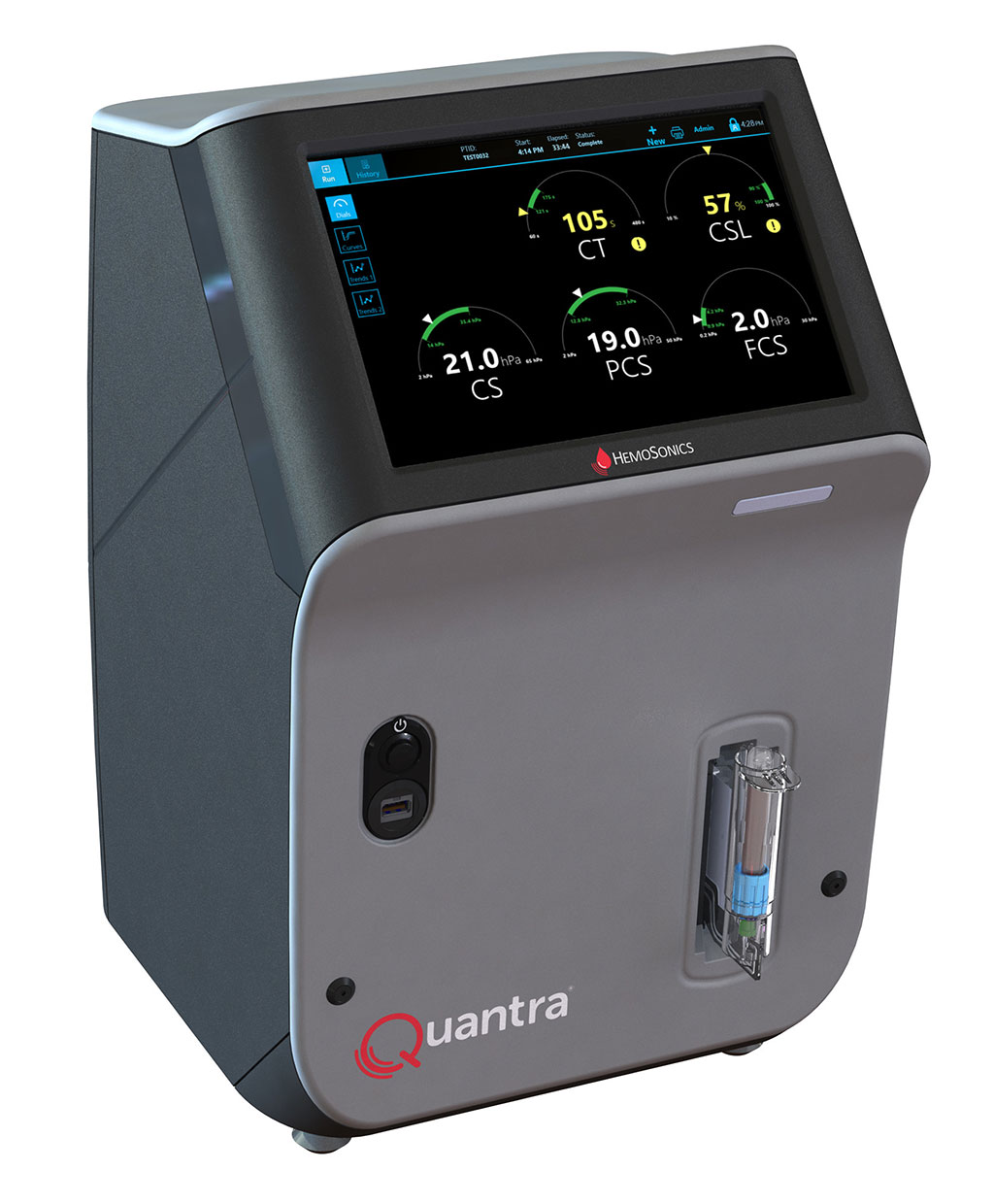
- Sistema de hemostasia de sangre total POC de última generación reconoce necesidades específicas de servicios de emergencia y quirófanos
- Laboratorio portátil permitirá identificación de infecciones bacterianas más rápida y económica en el punto de necesidad
- Mercado mundial de pruebas de cabecera será testigo de perspectivas prometedoras en cuidados intensivos
- Mercado mundial de diagnóstico de sepsis impulsado por el aumento de enfermedades adquiridas en hospitales

 Expo
Expo
- Interfaz de médula espinal restaura el control de la vejiga en estudio preclínico
- Sistema de control magnético permite la navegación precisa de dispositivos médicos miniaturizados
- Plaquetas sintéticas estables a temperatura ambiente podrían permitir el control prehospitalario de hemorragias
- Dispositivo de filtración sanguínea podría prolongar el embarazo en la preeclampsia temprana grave
- Sensor craneal no invasivo detecta el deterioro temprano en lesiones cerebrales agudas
- Nueva herramienta de IA predice complicaciones antes de la cirugía de cáncer de pulmón
- Dispositivo cardíaco de microcorriente menos invasivo mejora los resultados en insuficiencia cardíaca
- El trasplante parcial de corazón permite el reemplazo de válvulas con capacidad de crecimiento en niños
- Cirugía temprana de “entrenamiento cardíaco” promueve la regeneración en la insuficiencia cardíaca pediátrica
- Implante inteligente para fracturas monitoriza la curación y proporciona soporte adaptativo
- Dispositivo automático de lavado de vías intravenosas mejora la atención en infusiones
- Herramienta de capacitación en realidad virtual combate la contaminación de equipos médicos portátiles
- Plataforma de biosensores portátiles reducirá infecciones adquiridas en el hospital
- Tecnología portátil de luz germicida, única en su tipo, desinfecta superficies clínicas de alto contacto en segundos
- Solución de optimización de la capacidad quirúrgica ayuda a hospitales a impulsar utilización de quirófanos
- Sinocare presenta soluciones integradas de salud digital basadas en IA en CMEF
- GE HealthCare y Medtronic amplían su alianza con la integración de imágenes intraoperatorias.
- GE HealthCare lidera una importante iniciativa europea para impulsar la atención cardio-oncológica
- Philips y Masimo se asocian para impulsar las tecnologías de monitorización de pacientes
- B. Braun adquiere la empresa de microcirugía digital True Digital Surgery
- Herramienta basada en HCE predice el fallo del injerto tras un trasplante de riñón
- Nanopartículas imprimibles permiten la producción masiva de biosensores portátiles
- Los relojes inteligentes podrían detectar la insuficiencia cardíaca congestiva
- Un parche inteligente versátil combina monitoreo de salud y administración de fármacos
- Modelo de aprendizaje automático mejora predicción del riesgo de mortalidad para pacientes de cirugía cardíaca
- China aprueba la primera vacuna inhalable contra la COVID-19 del mundo
- Vacuna en parche contra la COVID-19 combate variantes del SARS-CoV-2 mejor que las agujas
- Pruebas de viscosidad sanguínea predicen riesgo de muerte en pacientes hospitalizados con COVID-19
- ‘Computadora Covid’ usa IA para detectar COVID-19 en exámenes de TC de tórax
- Técnica de resonancia magnética muestra la causa de los síntomas de COVID prolongada
- Sistema de hemostasia de sangre total POC de última generación reconoce necesidades específicas de servicios de emergencia y quirófanos
- Laboratorio portátil permitirá identificación de infecciones bacterianas más rápida y económica en el punto de necesidad
- Mercado mundial de pruebas de cabecera será testigo de perspectivas prometedoras en cuidados intensivos
- Mercado mundial de diagnóstico de sepsis impulsado por el aumento de enfermedades adquiridas en hospitales